O cobalto (Co) é um metal branco-acinzentado com propriedades magnéticas similares às do ferro e do níquel
O cobalto (Co) é um metal branco-acinzentado com propriedades magnéticas similares às do ferro e do níquel. Ele é relativamente raro e ocorre na natureza associado a outros minérios, como prata, chumbo e cobre. De modo geral, o cobalto é um elemento químico essencial para vários seres vivos, incluindo os humanos. Entretanto, ele pode se tornar tóxico em altas concentrações.
Todas as substâncias que interagem com os seres vivos, quando em excesso, podem se tornar tóxicas. O cobalto, assim como todos os micronutrientes essenciais, apresenta duas zonas de exposição incompatíveis com a vida: tanto a deficiência como o excesso podem levar à doença ou à morte.
Propriedades
O cobalto apresenta diversas propriedades. Entre elas, estão:
- Símbolo: Co;
- Número atômico: 27;
- Eletronegatividade: 1,88;
- Ponto de fusão: 1495 ºC;
- Densidade: 8900 kg/m3 ;
- Massa atômica: 59 u.m.a;
- Ponto de ebulição: 2900 ºC;
- Isótopos: 59Co (natural) e 60Co (sintético);
- Classificação: metal de transição externa;
História do cobalto
Minérios de cobalto vêm sendo usados há quase cinco mil anos, como constatado em artefatos de cerâmica egípcia, em vidros pérsicos e em vidros e porcelanas chinesas das dinastias Tang (618-907) e Ming (1368-1644). Além disso, a esmaltita é utilizada como pigmento cerâmico para a tonalidade azul há vários séculos.
O cobalto metálico foi isolado pela primeira vez em 1735 pelo químico sueco Georg Brandt a partir de uma amostra de esmaltita.
Onde encontrar?
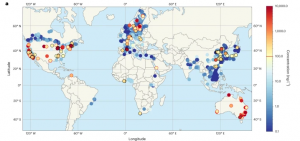
O cobalto ocorre na crosta terrestre na faixa de 0,001-0,002%, onde é encontrado na forma de minérios, tais como a cobaltita (CoS2.CoAs2), a linaeita (Co3S4), a esmaltita (CoAs2) e a eritrita (3CoO.As2O5.8H2O). Além disso, o cobalto é um componente central da vitamina B12 (cianocobalamina).
Essa vitamina participa de alguns processos bioquímicos importantes, tais como a síntese de aminoácidos e ácidos nucleicos e a formação de eritrócitos (hemácias ou glóbulos vermelhos do sangue). A ausência ou deficiência na ingestão dessa vitamina pode causar a anemia perniciosa (sintomas característicos: fraqueza, fadiga, diarreia, icterícia, adormecimento e formigamento dos pés e das mãos – parestesia) ou mesmo lesão cerebral.
Consequentemente, a vitamina B12 é um foco de preocupação no caso de dietas vegetarianas estritas, uma vez que ela só é encontrada em alimentos de origem animal. Nesses casos, a compensação da pouca ingestão de vitamina B12 pode ocorrer por suplementos orais ou injeções.
Aplicações do cobalto
O cobalto ainda é amplamente utilizado pelas indústrias de tinta e cerâmica para a produção de pigmentos azul e branco. Além disso, ele é usado para a fabricação de ligas de aço magnéticas, como a alnico, e como catalisador de reações químicas orgânicas. O cobalto também é utilizado para tratar câncer, pois emite radiações ionizantes capazes de destruir determinadas células.
Estudos sugerem que o cobalto possui um alto potencial para substituir a platina na produção de hidrogênio verde, barateando o processo.
Vias de exposição e efeitos
Quando somos expostos a níveis agudos de cobalto no ar, seja por meio do metal puro pulverizado, seja por poeiras de sais e óxidos de cobalto, podemos ter o desenvolvimento de problemas respiratórios, como diminuição da ventilação, congestão, edemas e hemorragias. Ainda, é possível que se observe inflamações da nasofaringe e efeitos alérgicos, como rinite alérgica e dermatite atópica (nesse caso, quando a exposição se dá pela pele).
A ingestão de cobalto, por sua vez, pode provocar efeitos gastrointestinais, como náusea, vômito e diarreira, alterações no fígado e dermatite alérgica. Por fim, a Agência Internacional de Pesquisa em Câncer classifica o cobalto e seus compostos como possíveis cancerígenos para o ser humano (Grupo 2B).