Cientistas brasileiros criam molécula que pode originar medicamento mais eficaz
Por Gilberto Stam em Revista Pesquisa Fapesp — Em busca de um analgésico mais eficaz e com menos efeitos colaterais, uma equipe de 18 pesquisadores brasileiros e um norte-americano resolveu estudar os portadores de uma doença genética que atinge apenas uma em cada 125 milhões de pessoas no mundo, chamada insensibilidade congênita à dor com anidrose (Cipa). Como não sentem dor ou calor, as pessoas com essa condição não conseguem reagir com prontidão diante de situações que podem causar danos, como doenças ou queimaduras. Além disso, não suam, sofrendo aumentos excessivos de temperatura. Ao compreender o que impede essas pessoas de sentirem estímulos dolorosos, os pesquisadores identificaram uma nova estratégia de analgesia e criaram um composto experimental capaz de reduzir a dor. Se avançar, o estudo poderá ajudar a tratar a dor crônica, que atinge cerca de um terço da população mundial e que pode levar à incapacidade de trabalhar, à depressão e ao transtorno de ansiedade, segundo a Sociedade Brasileira para Estudo da Dor (SBED).
“Acreditávamos que, entendendo melhor o mecanismo de uma doença que bloqueia a dor, poderíamos encontrar vias de sinalização úteis na formulação de novos analgésicos”, explica a bioquímica Deborah Schechtman, do Instituto de Química da Universidade de São Paulo (IQ-USP) e coordenadora do estudo, que ganhou a capa da edição de 26 de abril da revista Science Signaling.
O passo inicial era entender melhor por que uma proteína chamada receptor de tropomiosina quinase A (TrkA) não funciona nos portadores de Cipa, bloqueando o sinal nervoso da dor. Depois de elucidarem as falhas nesse mecanismo, os pesquisadores formularam e desenvolveram uma molécula capaz de superar o problema. “Criamos um analgésico que diminuiu sensivelmente a dor em testes feitos em camundongos”, comemora Schechtman.
Esse novo analgésico atua nos chamados nociceptores, neurônios comuns em tecidos ou órgãos expostos a estímulos que possam causar dor, como pele, músculos, estômago e intestinos. Ao ser acionado, o neurônio estimula a produção de uma substância chamada Fator de Crescimento Neural (NGF), que se liga ao receptor TrkA. Em seguida, o neurônio dispara o impulso elétrico que segue por um nervo até as regiões do cérebro que interpretam a dor e contribuem para fazer a pessoa reagir antes mesmo de ter consciência, se afastando do que causa a dor (uma queimadura, por exemplo).
“A vantagem dessa abordagem é mirar mecanismos específicos que causam dor em diferentes condições”, esclarece o farmacologista Thiago Mattar Cunha, da Faculdade de Medicina da USP de Ribeirão Preto (FMRP), que não participou do trabalho. Algumas décadas atrás, cientistas e empresas pensavam que havia um único mecanismo de dor, que opioides, analgésicos tradicionais ou anti-inflamatórios tratariam por meio de estratégias distintas. Hoje, sabe-se que a dor causada pelo diabetes, a inflamação crônica ou o câncer, por exemplo, funciona de formas distintas e nem sempre é detida pelos medicamentos à mão.
A dor crônica é tratada com vários fármacos que bloqueiam a transmissão do impulso no neurônio. “O ácido acetilsalicílico, mais conhecido por Aspirina, atua no local da inflamação, mas não em outros mecanismos de dor, enquanto os opioides têm um efeito geral, agindo no sistema nervoso central, mas com efeitos colaterais como sono e dependência. No caso da dipirona, princípio ativo da Novalgina, o mecanismo de ação não é bem conhecido”, ressalta Cunha, enfatizando a necessidade de analgésicos mais específicos.
Encruzilhada bioquímica
Bloquear a região da TrkA em que o NGF se conecta seria, portanto, a opção teoricamente mais eficaz para eliminar a dor. O problema é que, como o nome sugere, o NGF tem outra função importante: estimular o crescimento dos neurônios e a regeneração do tecido nervoso após algumas lesões. Por isso, os poucos medicamentos que bloqueiam a ação do NGF têm muitos efeitos colaterais. Se ele não atua, não há dor, mas podem ocorrer problemas de desenvolvimento do cérebro e transtornos cognitivos.
“Precisávamos de uma alternativa, uma via de sinalização que bloqueasse o impulso da dor, mas não o crescimento dos neurônios”, explica a bióloga Camila Squarzoni Dale, do Instituto de Ciências Biomédicas da USP, que também participou do trabalho. A resposta a esse dilema estava nas pessoas com Cipa.
A equipe da USP listou as mutações associadas à doença, identificadas em 230 pessoas nos últimos 50 anos em estudos feitos no mundo inteiro. Quatro delas tinham mutações que bloqueavam apenas uma via de sinalização mediada pelo NGF, a da enzima fosfolipase C, e um dos pacientes que tinha sintomas mais leves sentia um pouco de dor. “Isso sugeria que eles tinham uma mutação que afetava apenas a via de sinalização da dor, indicando novos caminhos para controlar a dor”, comenta Schechtman.
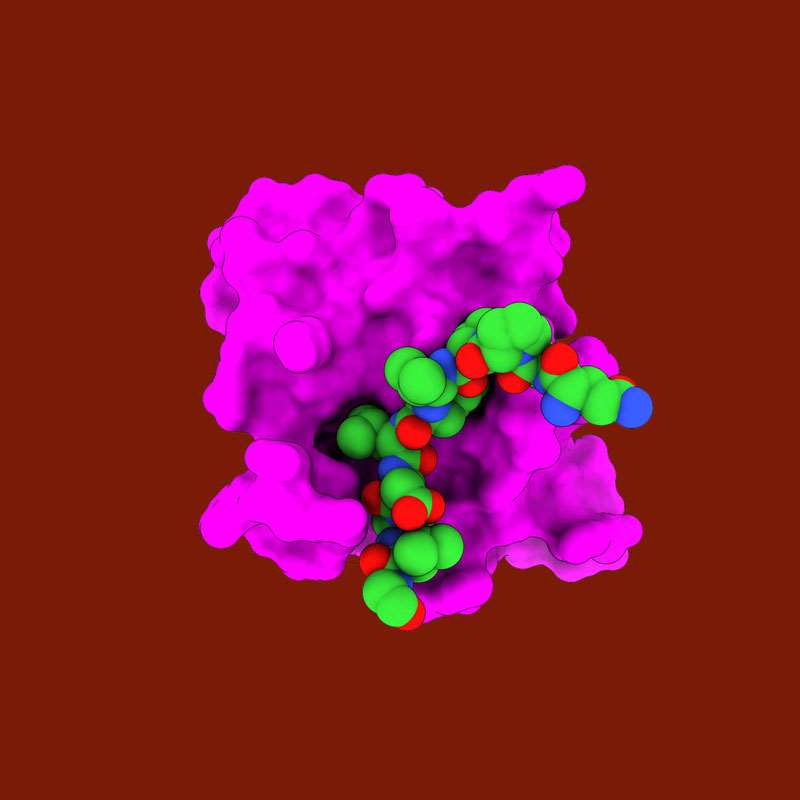
Para descobrir o efeito da mutação apresentada por cada paciente sobre o funcionamento da TrkA, os pesquisadores criaram modelos tridimensionais desses receptores nos computadores do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM), em Campinas, e realizaram testes virtuais para ver como eles interagiam com outras moléculas dentro e fora dos neurônios que percebem a dor. Um estudo anterior indicava que uma das moléculas ativadas pelo TrkA é a fosfolipase C, mas os pesquisadores não sabiam qual era o papel dela em diferentes tipos de dor. Além disso, essa proteína não parece afetar o crescimento e a regeneração dos neurônios.

Com base nessas observações, o grupo desenvolveu e sintetizou uma molécula, batizada como TAT-pQYP, que se liga ao TrkA no lugar da fosfolipase C, impedindo sua ação e reduzindo a dor. Nos experimentos, os camundongos receberam, nas patas traseiras, uma injeção que causava inflamação e dor. Depois, um aparelho mediu a intensidade da reação mecânica dos animais ao toque, que foi 40% maior após a aplicação do TAT-pQY. Os eventuais efeitos colaterais da substância não foram ainda estudados.
“É um trabalho elegante, completo e bem-feito, que faz o estudo do mecanismo molecular que causa a Cipa, a modelagem por computador e o desenvolvimento de uma molécula”, avalia Cunha. Mas ele alerta: “Entre a substância experimental e o remédio comercializado há um longo caminho, que nem sempre dá resultado”. Duas questões dificultam que a TAT-pQYP se torne um medicamento para tratar a dor. A molécula é muito complexa, o que dificulta sua produção pela indústria farmacêutica, além de grande.
Agora o grupo planeja identificar qual tipo de dor pode ser tratada pelo bloqueio dessa via. O objetivo é desenvolver as bases de um medicamento para a dor crônica com menos efeitos colaterais que os opioides, que, por gerar dependência, se tornaram um problema de saúde pública nos Estados Unidos. Nessa primeira etapa, a equipe contou com o apoio FAPESP, da Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (Capes) e do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq). As empresas farmacêuticas têm interesse na questão, trata-se de disputar um mercado que movimenta cerca de R$ 2,6 bilhões no país.
Em sua coluna de abril na Science sobre desenvolvimento de drogas, o químico Derek Lowe, da Novartis, alertou sobre a dificuldade de desenvolver novos analgésicos. Ele comentou sobre um trabalho anterior ao do grupo de Schechtman, em estágio mais avançado de desenvolvimento, com uma proteína dos neurônios chamada Nav 1.7, importante na geração e transmissão do sinal nervoso, especialmente nos neurônios da dor. Segundo ele, foi possível elaborar compostos para bloquear a Nav 1.7, mas “nenhum deles mostrou eficácia significativa”. Como Lowe escreveu, o desenvolvimento de analgésicos é uma rocha que já fez muitos navios naufragarem, embora tragam novos conhecimentos sobre a origem de um mecanismo fundamental.
Projetos
1. Caracterização e desenvolvimento de novos moduladores das vias da TrkA e PKMzeta na dor inflamatória e crônica (nº 19/06982-6); Modalidade Projeto Temático; Pesquisadora responsável Deborah Schechtman (USP); Investimento R$ 1.810.565,34.
2. Detecção e caracterização de cavidades proteicas através de computação paralela e descritores moleculares (nº 18/00629-0); Modalidade Auxílio à Pesquisa ‒ Regular; Pesquisador responsável Paulo Sergio Lopes de Oliveira (CNPEM); Investimento R$ 83.888,63.
3. Regulação da proteostase de MST2 na via Hippo (nº 19/26767-2); Modalidade Auxílio à Pesquisa ‒ Regular; Pesquisador responsável Alexandre Bruni Cardoso (USP); Investimento R$ 231.309,28.
4. Efeito de mutações no gene TrkA encontradas na insensibilidade à dor congênita sobre vias de sinalização celular (nº 18/07201-5); Modalidade Bolsa de Mestrado; Convênio Capes; Pesquisadora responsável Deborah Schechtman (USP); Bolsista Beatriz Caroline de Moraes; Investimento R$ 46.057,80.
5. Identificação de proteínas alvo da pkc¹/» e vias de sinalização em tumor de pâncreas (nº 17/14696-8); Modalidade Bolsa de Pós-doutorado; Pesquisadora responsável Deborah Schechtman (USP); Bolsista Damian Emilio Berardi; Investimento R$ 206.258,86.
6. Mecanismos de regulação da expressão da proteína quinase C atípica PKMZ, e identificação do seu interactoma em contextos neurais específicos (nº 15/17812-3); Modalidade Bolsa de Doutorado; Pesquisadora responsável Deborah Schechtman (USP); Bolsista Dimitrius Tansini Pramio; Investimento R$ 177.167,54.
7. Fotobiomodulação como terapia complementar no tratamento de feridas diabéticas: Efeitos sobre a sensibilidade dolorosa exteroceptiva, processo de cicatrização e possíveis mecanismos moleculares (nº 18/18483-1); Modalidade Bolsa de Doutorado; Pesquisadora responsável Camila Dale (USP); Bolsista Victória Regina da Silva Oliveira; Investimento R$ 283.089,13.
Artigos científicos
MORAES, B. C. Structural analysis of TrkA mutations in patients with congenital insensitivity to pain reveals PLCγ as an analgesic drug target. Science Signaling. v. 15, n. 731. 26 abr. 2022 SOUZA, J. B. Prevalence of chronic pain, treatments, oerception, and interference on life activities: Brazilian population-based survey. Pain Research and Management. On-line. 26 set. 2017
Este texto foi originalmente publicado por Revista Pesquisa Fapesp de acordo com a licença Creative Commons CC-BY-NC-ND. Leia o original. Este artigo não representa necessariamente a opinião do Portal eCycle.